JARDIANCE®
Kroonisen munuaistaudin hoitoon*

JARDIANCE® tarjoaa suojaa potilaille, joilla on krooninen munuaistauti1
- tutkittu laajimmalla potilaspopulaatiolla SGLT2-estäjien luokassa2
- EMPA-KIDNEY -tutkimuksessa mukana myös ei-albuminurisia potilaita2
- matalin eGFR-aloitustaso 20ml/min/1,73m2 SGLT2-estäjien luokassa – kaikissa käyttöaiheissa1
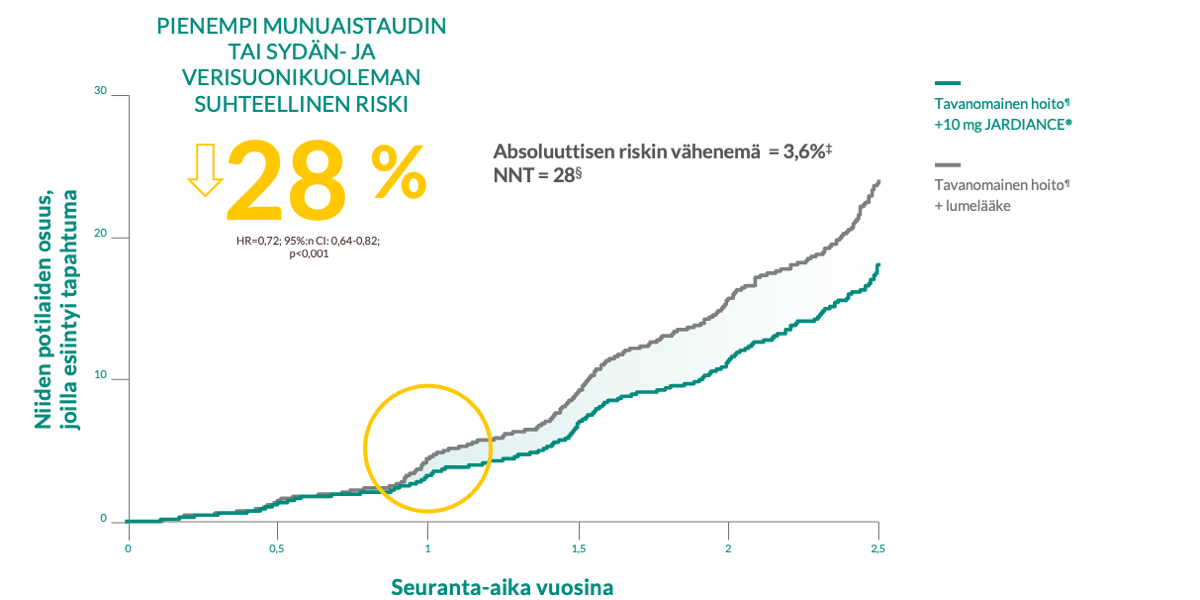
JARDIANCE® PIENENSI MUNUAISTAUDIN ETENEMISEN TAI SYDÄN- JA VERISUONIKUOLEMAN RISKIÄ KROONISTA MUNUAISTAUTIA SAIRASTAVILLA POTILAILLA RIIPPUMATTA SIITÄ, OLIKO HEILLÄ TYYPIN 2 DIABETES VAI EI*†1,2
Alaviitteet
-
*
Aikuiset potilaat, joilla eGFR ≥ 20, < 45 ml/min/1,73m2; tai eGFR ≥ 45, < 90 ml/min/1,73m2 ja U-AlbKrea ≥ 200 mg/g.
-
†
EMPA-KIDNEY oli satunnaistettu, kaksoissokkoutettu, rinnakkaisryhmissä toteutettu lumekontrolloitu tutkimus, jossa arvioitiin JARDIANCE® 10 mg -valmisteen (n = 3 304) tehoa ja turvallisuutta verrattuna lumelääkkeeseen (n = 3 305) 6 609 potilaalla, joilla oli krooninen munuaistauti. Ensisijainen päätetapahtuma EMPA-KIDNEY-tutkimuksessa oli sydän- ja verisuonikuoleman ja munuaistaudin etenemisen yhdistelmätapahtuma. Munuaistaudin etenemisen määritelmänä oli loppuvaiheen munuaisten vajaatoiminta (ylläpitodialyysin aloittaminen tai munuaisensiirto), eGFR pysyvästi < 10 ml/min/1,73 m2, pysyvä ≥ 40 %:n eGFR:n lasku lähtötilanteesta tai munuaisperäinen kuolema. JARDIANCE®-hoitoa saaneilla potilailla tämän päätetapahtuman suhteellinen riski pieneni 28 % (HR = 0,72; 95 %:n LV: 0,64, 0,82; p < 0,001).
-
‡
Ensisijaisen yhdistelmätapahtuman eli munuaistaudin etenemisen tai sydän- ja verisuonikuoleman absoluuttisen riskin vähenemä on 3,6 % riskipotilasvuotta kohti. Kuva muokattu julkaisusta Herrington ym.
-
§
NNT: 28 (95 %:n LV: 19,53) 2 riskivuotta kohti.
-
¶
Tavanomainen hoito: Kaikki potilaat saivat reniini-angiotensiini-aldosteronijärjestelmää (RAAS) estävää lääkitystä, paitsi jos tutkijan harkinnan mukaan tällainen lääkitys ei ollut aiheellista tai siedettyä.
-
eGFR = glomerulusten laskennallinen suodatusnopeus, HR = riskisuhde; LV = luottamusväli; NNT = Number Needed to Treat (potilaiden määrä, joka pitää hoitaa, jotta yksi potilas hyötyisi hoidosta); U-AlbKrea = albumiinin ja kreatiniinin suhde virtsassa.
Lähteet
-
Jardiance valmisteyhteenveto
-
Herrington WG, Staplin N, Wanner C ym. EMPA-KIDNEY Collaborative Group. Empagliflozin in patients with chronic kidney disease. N Engl J Med. 2023;388(2):117–127. (EMPA-KIDNEY-tutkimuksen tulokset ja julkaisun täydennysliite)
EMPA-KIDNEY
Lue lisää
Käyttötarkoitus
JARDIANCE® on tarkoitettu tyypin 2 diabeteksen hoitoon aikuispotilaille, joilla sairaus ei ole riittävässä hoitotasapainossa, liikunnan ja ruokavaliohoidon ohella
- monoterapiana, kun metformiinia ei sietokyvyttömyyden takia pidetä sopivana vaihtoehtona
- muiden diabeteksen hoitoon tarkoitettujen lääkevalmisteiden lisänä.
JARDIANCE® on tarkoitettu oireisen kroonisen sydämen vajaatoiminnan hoitoon aikuisille.
JARDIANCE® on tarkoitettu kroonisen munuaistaudin hoitoon aikuisille.
Alaviitteet
-
*
EMPA-KIDNEY oli satunnaistettu, kaksoissokkoutettu, rinnakkaisryhmissä toteutettu lumekontrolloitu tutkimus, jossa arvioitiin JARDIANCE® 10 mg -valmisteen (n = 3 304) tehoa ja turvallisuutta verrattuna lumelääkkeeseen (n = 3 305) 6 609 potilaalla, joilla oli krooninen munuaistauti. Ensisijainen päätetapahtuma EMPA-KIDNEY-tutkimuksessa oli sydän- ja verisuonikuoleman ja munuaistaudin etenemisen yhdistelmätapahtuma. Munuaistaudin etenemisen määritelmänä oli loppuvaiheen munuaisten vajaatoiminta (ylläpitodialyysin aloittaminen tai munuaisensiirto), eGFR pysyvästi < 10 ml/min/1,73 m2, pysyvä ≥ 40 %:n eGFR:n lasku lähtötilanteesta tai munuaisperäinen kuolema. JARDIANCE®-hoitoa saaneilla potilailla tämän päätetapahtuman suhteellinen riski pieneni 28 % (HR = 0,72; 95 %:n LV: 0,64, 0,82; p < 0,001).
PC-FI-103794-META-08-2025
